Research Activity
研究紹介高血圧・血管不全グループ
- 2021.06.1 |
<高血圧および高血圧性臓器障害に関する研究>
1. 高血圧性心不全(とくに左室収縮保持性心不全)に関する研究
近年、高齢者心不全の多くが左室収縮機能が保持されていながら拡張機能障害を主体とする左室収縮保持性心不全(heart failure with preserved ejection fraction; HFpEF)であることが明らかとなり、未曾有の高齢化社会を迎える本邦での“心不全パンデミック”の多くはHFpEF患者であると予想されています。HFpEFの多くの発症基盤には高血圧があり、収縮性心不全と同様に予後不良であること、確立した治療法が全くないことから大きな問題となっており、その発症・病態進展機序の解明、新たなリスク層別化マーカーの確立、予後改善のための治療法の開発が急務となっています。
1)酸化ストレスに着目した左室収縮保持性心不全の病態機序解明のための基礎・臨床研究
われわれはこれまで、食塩負荷により血管内皮機能障害から心拡張不全を発症するDahl食塩感受性(DS)ラットを用いて、様々な経路を介した酸化ストレス(ROS)の増加が高血圧による血管内皮機能障害とHFpEFの発症と進展に深く関与していることを報告しています(Yamamoto E, et al. Arterioscler Thromb Vasc Biol. 2007, Arterioscler Thromb Vasc Biol. 2007, Hypertension 2007)。現在も、同モデル動物を用いてROSやROS誘導性分子に着目して新たなHFpEFの分子機序解明を目標とした基礎研究を推進しています。
また臨床研究においても、血中酸化ストレスレベルの新たな測定ツールであるDROM(derivatives of reactive oxygen metabolites)を用いて、HFpEF患者では血管内皮機能障害が惹起されていると同時に全身のROSレベルも増加していること、その機序に内皮型一酸化窒素合成酵素(eNOS)の機能異常が関与していることを臨床的に証明しています(Akiyama E, et al. J Am Coll Cardiol. 2012, Hirata Y, et al. Int J Cardiol. 2014, Yamamoto E, et al. Int J Cardiol. 2015, ESC heart Fail. 2016)。さらにその一環で、左室収縮低下型心不全(heart failure with reduced ejection fraction; HFrEF)患者におけるDROMの意義に関しても検討を行っており、DROMがHFrEFにおいて冠循環において産生され有用な予後予測マーカーにもなりえること(Nishihara T, et al. J Card Fail. 2021)、非虚血性HFrEFにおけるリバースリモデリングのマーカーとしてもDROMが有用なこと(Nishihara T, et al. J Am Heart Assoc. 2021)を報告しています。
2)左室収縮保持性心不全のリスク層別化のためのバイオマーカーの確立
前述のようにHFpEFはHFrEFと同様に予後不良であることから新たな簡便なリスク層別化のツールの確立が待望されています。HFpEFはHFrEFとは異なる病態と理解され心臓単独の疾患ではなく心臓と動脈系の相互作用から惹起されるという概念が提唱されていることから、われわれは血管機能評価がHFpEFにおける有用な予後予測マーカーとなり得ると仮説し、様々なモダリティを用いてその有用性を明らかにしています(Akiyama E, et al. J Am Coll Cardiol. 2012, Tokitsu T, et al. Eur J Heart Fail. 2016, J Hypertens. 2017, Takae M, et al. Am J Hypertens. 2019)。さらに血管傷害マーカーだけではなく、様々な新しいバイオマーカーの慢性心不全における意義についても多面的に評価し、その成果を報告しています(Kusaka H, et al. Circ J. 2015, Nishihara T, et al. Am J Hypertens. 2018, Am J Respir Crit Care Med. 2019, Fujisue K, et al. Medicine (Baltimore) 2019, Sueta D, et al. Am J Hypertens. 2019, Takae M, et al. ESC Heart Fail. 2021)。
3)左室収縮保持性心不全の新たな治療法確立のための臨床研究
HFpEFはその病態機序が詳細には分かっていないことから、現時点では確立した治療法が乏しい点が大きな問題点になっています。これまで様々な大規模臨床試験で、主にHFrEFを対象に有効性が証明された薬剤のHFpEFに対する効果が検討されましたが、いずれの薬剤もはっきりとした有用性は証明されませんでした。しかし、これら大規模臨床試験の“失敗”には対象患者のセレクションバイアスなどプロトコル上の問題が指摘されています。
我々は当科単施設の小規模の研究ながら、AT1受容体拮抗作用の比較的強い、AT1受容体拮抗薬(ARB)であるolmesartanが高血圧性のHFpEF患者の末梢血管内皮機能のみならず心拡張能を改善させることを明らかにしました(ORION研究:Yamamoto E, et al. Int J Cardiol Heart Vasc. 2015)。 また、当科関連の多施設と協力して、高血圧性HFpEF患者に対するミネラルコルチコイド受容体拮抗薬(MRA)であるeplerenoneの有効性を検討する大規模臨床試験:MELODY試験を行いました。本試験は目標登録数に達し研究を終了しており、現在結果を解析中です。
2. 高血圧における心腎連関に関する基礎・臨床研究
心不全は同時に腎臓病を悪化させ、腎臓機能の低下(慢性腎臓病)は心臓病を増やしたり悪化させます。この現象を“心腎連関”といい、高血圧では心臓と腎臓がいろいろなメカニズムでお互いに関連し合っていると考えられています。前述のDSラットは高食塩負荷で高血圧性心不全をきたすとともに早期よりアルブミン尿を伴う慢性腎臓病(CKD)を呈し、いわば“心腎連関”モデルでもあるといえます。我々は以前よりこのモデル動物を使って基礎的に心臓-腎臓をつなぐ新しい臓器のネットワークを検討しています(Yamamoto E, et al. Hypertension. 2007, J Hypertens. 2010)。また、臨床研究においては、ROSの増加が高血圧におけるCKDや虚血性心臓病の病態にともに深く関与していることを明らかにしています(Hirata Y, et al. Medicine (Baltimore) 2015, J Am Heart Assoc. 2015)。
3. 腎神経デナベ-ションに関する臨床ならびに基礎研究
従来から、本態性高血圧の成因における交感神経活動の亢進の重要性は数多くの研究から明らかにされてきました。腎臓においては、腎虚血、低酸素、腎実質障害により求心性の腎交感神経が亢進し、脳内では最終的に頭側延髄腹外側野ニューロン活性化から遠心性の腎交感神経を介して血圧がさらに上昇するという悪循環が形成されていることが知られており、基礎研究においては、腎神経を物理的・化学的に切断することにより交感神経活動の亢進を 抑制し高血圧のみならず、それによる様々な全身の臓器での循環制御や臓器障害を改善させることがしめされています。われわれも様々な高血圧モデル動物を用いた基礎研究(下図)で、腎神経の切離によりROSの抑制と血管内皮機能が改善し、心筋肥大や線維化が抑制されることをこれまでに明らかにしています。
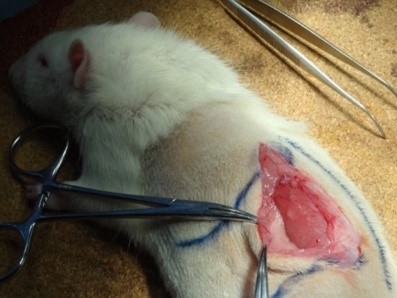
昨今、臨床の分野でも経カテーテル的に腎求心性ニューロンと遠心性ニューロンを含む交感神経を焼灼する、いわゆる“腎神経デナベーション(RDN)術”が応用され、主に治療抵抗性高血圧患者に対する新しいコンセプトの治療としておおきな注目を浴びています。当科でも本邦で実施されているRDNの治験2つに参加し治療抵抗性高血圧患者に対するRDNを積極的に行っており(Kario K, Yamamoto E, et al. Circ J. 2019)、おもに血管機能に着目した臨床研究によりRDNの効果予測ツールの開発を目指しています。
メンバー紹介
山本 英一郎(診療講師)
末田 大輔 (特任講師)
藤末 昂一郎(助教)
尾池 史 (医員)
小森田 貴史(特任助教)
江頭 興一 (大学院生)
連携研究者
宇宿 弘輝 (助教)
高潮 征爾 (助教)
<動脈硬化・血管機能に関する研究>
血管内皮は血管内腔を覆う細胞で、様々な生理活性物質の分泌、調整により人体の恒常性を維持しています。血管内皮は全身のありとあらゆる血管に存在しており、人体最大の内分泌臓器といえます。血管内皮障害は動脈硬化性疾患、心不全、不整脈といった心血管疾患の病態に関連しており、血管内皮機能の適切な評価とそれを指標とした治療開発が世界的に待望されております。私たちの研究グループでは以下のようなアプローチで血管内皮をはじめとした血管機能の評価を行い、心血管疾患に対する新たな診断法や治療法開発につながる研究を目標に検討を行っています。
1. 侵襲的冠動脈内皮機能検査(アセチルコリン負荷試験による)
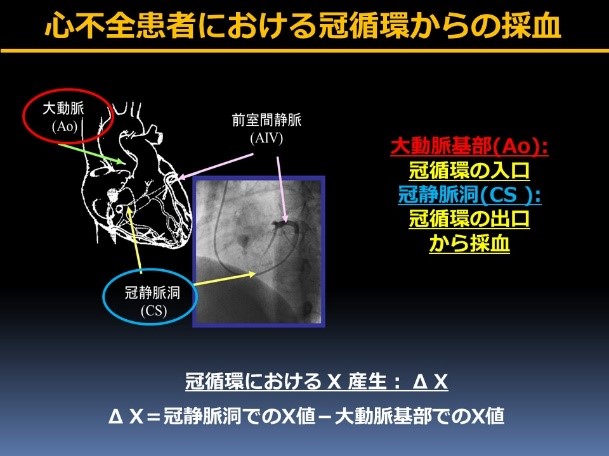
私たちは当科で確立した冠動脈アセチルコリン負荷試験の手法を用いて冠動脈血管内皮機能障害を生理学的に評価し、様々な心血管疾患病態への関与を明らかにしてきました(Nakamura S, et al. Circulation 2003, Koga H, et al. J Am Coll Cardiol. 2005, Matsuzawa Y, et al. J Am Coll Cardiol. 2010, Ohba K, et al. J Am Heart Assoc. 2012, Takae M, et al. Int J Cardiol. 2018)。当科での冠動脈アセチルコリン負荷試験という手法には長い歴史があり、生理学的な血管内皮細胞機能検査として最も確立された検査といえます。また同時に挿入したカテーテルにより心臓内の各部位から血液採取することで(下図)、冠循環・心臓内からの様々なホルモンやサイトカイン産生を測定しており、ホルモン産生臓器としての心臓という側面と冠動脈血管内皮機能障害、冠微小循環との関わりについても興味深い知見をえております。
2. 非侵襲的血管内皮機能検査
私たちはReactive hyperemia peripheral arterial tonometry (RH-PAT)(下図) を用いて非侵襲的に末梢血管内皮機能を測定し、様々な心血管疾患における役割を検討しています。RH-PATは特殊なプローブを指先に装着し、対照側の片腕と対側の腕を駆血し駆血解除後の脈波の変化を血管拡張反応としてコンピュータで自動計測します。本検査で得られた値は、客観的で再現性高く検査結果を得られるため、検者の技術に影響されることなく全世界的に標準化された定量的データとして多施設間比較検討が可能で、前述の冠動脈アセチルコリン負荷試験により評価した冠動脈血管内皮機能障害の程度とも良好な相関があることが分かっております。

私たちは安定冠動脈疾患患者において、RH-PAT値で評価される末梢血管内皮機能低下が血小板凝集能亢進と関連すること(Fujisue K, et al. Circ Cardiovasc Interv. 2013)、左室収縮能の低下した心不全患者において低RH-PAT値がその後のイベントの予測因子になること(Fujisue K, et al. Circ J. 2017)を報告してきました。また、これまでも冠動脈疾患を含む動脈硬化性疾患や高血圧性の心不全などの各種循環器疾患における病態評価、予後予測におけるRH-PATの有用性に関して多数の報告をしております(Matsuzawa Y, et al. J Am Coll Cardiol. 2010, Akiyama E, et al. J Am Coll Cardiol. 2012, Matsuzawa Y, et al. Circ J. 2013, Hirata Y, et al. Int J Cardiol. 2014, Maeda H, et al. J Cardiol. 2016, Sumida H, et al. J Cardiol. 2017)。現在も各種循環器疾患患者においてRH-PAT測定を継続しており末梢血管内皮機能を指標とした心血管疾患の病態評価や新たな治療方法の開発を推進しています。
さらに私たちはAnkle Brachial index (ABI) deviceを用いた非侵襲的血管機能検査も精力的に行っており、これらで測定した各種パラメーター(上腕血圧左右差:Tokitsu T, et al. J Hypertens. 2015、poly-vascular disease合併:Maeda H, et al. J Cardiol. 2016, Fujisue K, et al. Medicine (Baltimore). 2019、脈圧:Tokitsu T, et al. Eur J Heart Fail. 2016、baPWV: Tokitsu T, et al. J Hypertens. 2017, Tabata N, et al. J Hypertens. 2019, Takae M, et al. Am J Hypertens. 2019)が様々な循環器疾患において有用な心血管イベントのリスクマーカーになることを明らかにしています。
メンバー紹介
山本 英一郎(診療講師)
末田 大輔 (特任講師)
藤末 昂一郎(助教)
尾池 史 (医員)
小森田 貴史(特任助教)
江頭 興一 (大学院生)
宮﨑 修平 (大学院生)
連携研究者
宇宿 弘輝 (助教)